1. 서 론
2. 실험방법
2.1 자테스트
2.2 응집능 지표 측정: 잔류 고형물 농도 및 응집체 크기
3. 실험결과 및 고찰
3.1 이온강도가 점토입자-생체고분자물질 응집에 미치는 영향
3.2. 2가 양이온이 점토입자-생체고분자물질 응집에 미치는 영향
3.3 휴믹물질이 생체고분자물질-부유입자 응집에 미치는 영향
4. 결 론
1. 서 론
하천, 호소, 하구, 연안 등 수자원환경에서의 응집은 점토, 미생물, 입자성 유기물 등 부유입자를 뭉쳐 응집체를 형성하게 하고, 응집체 크기, 침강속도에 따라 탁수 및 퇴적물의 운명을 결정하는 중요한 요소이다(Winterwerp and van Kesteren, 2004; Droppo, 2001; Maggi, 2009) 응집은 유속, 난류강도와 같은 수체 물리적 요인과, pH, 이온강도(Ionic Strength), 2가 양이온 농도, 수중 유기물 특성 및 농도 등 수질화학 조건에 의해 영향을 받는 것으로 알려져 있다(Chen et al., 2005; Mietta et al., 2009a, 2009b; Furukawa et al., 2014; Tang and Maggi, 2016). 예를 들어, 수체 흐름, 즉 유속 및 난류강도가 약한 경우, 응집이 증대되어 더 큰 응집체를 형성하고, 이와 반대로 수체 흐름이 강한 경우 응집체가 파괴하여 더 작은 응집체 및 개별 입자를 형성하는 것으로 알려져 있다(Maggi, 2005; Lee et al., 2014, Lee and Toorman, 2015).
응집은 수체 화학적 요인인 이온강도 및 2가 양이온 농도에 큰 영향을 받는다. 일반적으로 수중 미세 부유입자는 콜로이드로써 표면에 주로 음전하를 가지고 입자간 정전기적 반발력을 형성하게 된다. 이와 같은 입자간 정전기적 반발력은 응집을 방해하고 개별입자를 수체에 부유하게 한다(Stumm and Morgan, 1996). 하지만, 반발력을 가진 개별입자들이 하구 및 연안에 도달 할 경우, 해수의 높은 이온강도 영향으로 개별입자의 정전기적 반발력이 감쇄되어 입자간 응집을 증진시킨다. 특히, Ca2+, Mg2+와 같은 2가 양이온은 개별입자 표면에 직접 흡착하여 표면전하 및 정전기적 반발력을 감쇄하고 응집을 증진시킨다(Chassagne et al., 2009; Mietta, 2010). 수체에 고분자물질이 존재하는 경우, 2가 양이온은 부유입자-고분자물질 간 가교를 형성하여 응집을 크게 증대시키는 것으로 알려져 있다(Lee et al., 2012).
이온강도 및 2가 양이온 농도와 더불어, 수중유기물 특성 및 농도 역시 응집에 큰 영향을 미치는 것으로 알려져 있다. 수자원환경에서의 대표적인 수중유기물은 휴믹물질(Humic substances, HS)과 생체고분자물질(Extracellular polymeric substances, EPS)이 있다. 휴믹물질은 토양, 식생에서 지구-생화학적인 반응을 통해 발생이 되며 강우 유출시 수체로 유입된다. 휴믹물질은 벤젠링 구조를 포함하고 음전하를 띠며, 분자량이 비교적 작은 고분자물질에 해당한다. 휴믹물질은 점토 등 부유입자에 흡착이 될 경우 응집을 방해하고 입자를 안정화시키는 것으로 알려져 있다(Kretzschmar et al., 1998; Furukawa et al., 2014; Lee et al., 2017).
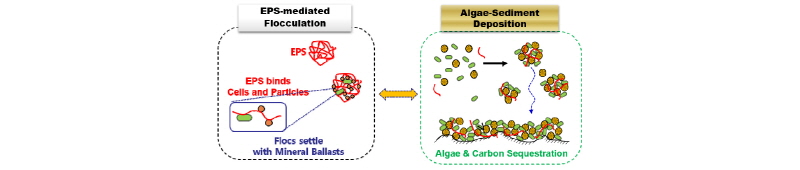
이에 반하여 생체고분자물질은 수중 미생물에 의해 수체에서 생산되는 것으로 알려져 있다. 특히, 부영양화, 녹조 발생 시기에 생체고분자물질이 다량 생산된다. 휴믹물질과 달리, 생체고분자물질은 사슬형태의 분자량이 아주 큰 고분자물질이며, 부유입자에 흡착할 경우 사슬형태의 긴 구조로 인하여 부유입자의 정전기적 반발력을 극복하고 입자간 가교를 형성하여 응집을 증진시킨다(Van der Lee, 2000; Lee et al., 2017) (Fig. 1). 생체고분자물질은 수체에 존재하는 점토, 미생물, 바이오매스 등 부유입자들을 응집을 통하여 큰 응집체를 형성하도록 부유입자들을 엮어주는 기능을 한다(Droppo et al., 2005; Maggi, 2013, Maggi and Tang, 2015). 이와 같은 복합 응집체는 쉽게 침강하여 하천 및 호소 바닥면으로 가라앉게 된다. 경우에 따라서는 저니층을 형성하여 수체의 수질 오염을 가중시키는 역할을 할 수 있다(Fig. 1). 생체고분자물질은 수체에서의 점토, 미생물, 바이오매스 등 부유입자들의 응집, 퇴적에 영향을 미치고, 결국 하천, 호수의 수질을 결정적 영향을 미치는 것으로 판단된다(Hwang et al., 2008).
본 연구는 이와 같은 생체고분자물질이 미세 부유입자 응집에 미치는 영향을 파악하고자 하였다. 특히, 이온강도, 2가 양이온 농도, 휴믹물질이 생체고분자물질과 물질과 함께 수체에 공존하는 경우, 이들 물질이 생체고분자물질에 의한 응집에 어떠한 영향을 미치는지 파악하고자 하였다. 일반적으로 2가 양이온은 음전하의 부유입자와 생체고분자물질 사이의 가교 역할을 하여 응집을 증진시키는 것으로 알려져 있고(Mietta, 2010; Lee et al., 2012), 휴믹물질은 부유입자에 흡착하여 추가적인 음전하 및 정전기적 반발력을 부여하여 응집을 방해하는 것으로 알려져 있다(Kretzschmar et al., 1998). 이온강도, 2가 양이온, 휴믹물질에 대한 수질화학 조건을 제어한 실험조건에서 생체고분자물질에 의한 미세 부유입자의 응집현상을 관측하여, 수자원환경에서 생체고분자물질에 의한 응집이 어떠한 기작으로 발생하는지 파악하고자 하였다.
2. 실험방법
2.1 자테스트
본 연구의 응집 실험은 Xanthan Gum (Sigma-Aldrich, USA)을 생체고분자물질의 대표로 사용하였고, 국내 하천 유역의 주요 점토 구성물질인 Kaolinite (Sigma-Aldrich, USA)를 부유입자의 대표로 사용하였다. 응집실험은 자테스터(Daihan Scientific Inc., Korea)를 활용하여 수행하였다. 먼저, 20 g/L Kaolinite 저장용액, 50 mg/L Xanthan Gum 저장용액, 그리고 희석용액을 각각 준비하였다. 모든 저장용액 및 희석용액은 충분히 용해, 안정화될 수 있도록 24시간 교반하였고, 표준 HCl, NaOH 용액을 투여하여 pH 7.0±0.2 로 조정하였다.
응집실험에서는 자테스터 6개 용기에 Kaolinite 농도가 2 g/L, Xanthan Gum 농도가 0.1, 0.5, 1.0, 5.0, 10, 30 mg/L가 되도록 Kaolinite 현탁액, Xanthan Gum 저장용액을 응집실험 시작과 동시에 혼합하였다. 250 rpm 속도로 1분간 급속 혼합 후, 50 rpm (속도경사 G = 30/s) 속도로 응집이 충분히 정상상태에 도달할 수 있도록 5시간 동안 완속 교반을 수행하였다. 완속 교반이 종료되기 직전, 응집체 샘플을 spatula를 이용하여 조심스럽게 채취하여 미리 준비한 한천용액에 고정하여 응집체 이미지에 사용하였다. 그리고 완속교반 종료 후, 1시간의 침전 시간을 두고 수체에 잔존 고형물 농도 측정을 위해 수표면 2 cm 지점에서 상등액을 채수하였다. 응집체 크기 및 잔존 고형물 농도는 수체 응집능 평가지표로써 활용 되었으며, 응집체 크기가 클수록 그리고 잔존 고형물 농도가 작을수록 수체의 응집능이 큰 것으로 나타난다.
본 연구에서는 이온강도, 2가 양이온 농도, 휴믹물질 농도를 실험변수로 조정하며 각 응집실험을 수행하였다. 먼저, 수체 이온강도가 생체고분자물질에 의한 부유입자 응집에 미치는 영향을 파악하기 위한 응집실험의 경우, 저장, 희석용액의 이온농도를 0.0001, 0.001, 0.01, 0.1 M NaCl 조건으로 보정하여 응집실험을 수행하였다. 또한, 2가 양이온 투여가 응집에 미치는 영향을 파악하기 위하여 0.001M NaCl 이온농도 조건에서, 100 mg/L Ca2+ 저장용액을 점토-생체고분자물질 현탁액에 투여하여 Ca2+ 농도가 0.1, 0.5, 1.0 mg/L가 되도록 조정하였다. 마지막으로, 휴믹물질이 응집에 미치는 영향을 평가하기 위하여, 0.001M NaCl 이온농도 조건에서 미생물 생체고분자물질(Extracellular Polymeric Substances, EPS)과 휴믹물질을 일정 비율(5, 20, 40% HA)로 함유한 저장용액과 Kaolinite 현탄액을 혼합하여 응집실험을 수행하였다.
2.2 응집능 지표 측정: 잔류 고형물 농도 및 응집체 크기
침전 후 수체에 잔류한 고형물 농도는 Standard Methods 2540D, Total Suspended Solids (APHA, 1998) 방법을 따라 측정을 하였다. 침전 후 채수된 상등액을 0.2 µm Supor® membrane filter (Pall Corp., US)에 걸러주고 상등액상 고형물을 포함한 필터를 105°C 24시간 건조 후, 데시케이터에서 2시간 방열 시켜주었다. 최종적으로 표면에 잔존하는 무게를 측정하여 상등액상 잔존 부유고형물 농도(mg/L)로 환산하였다.
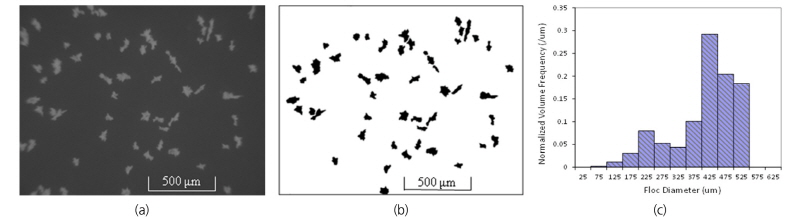
응집체 크기 및 형태는 응집체 고정, 사진 촬영, 이미지 분석 과정을 통하여 측정하였다. 5시간의 완속교반 종료 직전, 응집체를 채취하고 더 이상의 응집을 방지하기 위해 즉시 한천용액에 고정하였다(Gorczyca and Ganczarczyk, 1996; Lee et al., 2012). 한천용액에 고정된 응집체는 접사렌즈(SEL30M35, SONY, Japan)를 장착한 디지털 카메라(SONY α6000, Japan)를 사용하여 이미지를 촬영하였다. 원본 응집체 이미지는 ImageJ (National Institutes of Health, MD, USA) 이미지 프로세싱 프로그램을 활용하여 명암, 밝기 등을 조절하고, 수정된 이미지에 대하여 응집체 크기(Volume-averaged floc diameters)를 측정하였다(Fig. 2). 하지만, 디지털 카메라의 해상도의 한계로 20 µm 미만의 응집체는 분석대상에서 제외되었다. 본 분석법에서의 입자 크기 분포는 초기 점토입자 크기를 포함한 전 영역을 고려하지 않고, 20 µm 이상의 응집체만을 대상으로 한다는 점을 주의해야 한다. 대신, 잔류 점토입자는 앞서 소개한 침전 후 잔류 부유고형물 농도로 대표될 수 있다.
또한, 점토입자 및 응집체에 흡착된 생체고분자물질 량을 측정하기 위하여, 먼저 고액 분리를 위하여 10,000 g 속도로 20분 동안 Sorvall Evolution RC (Thermo Fisher Scientific Inc., USA)를 활용하여 원심분리를 수행하였고, 수체에 잔존하는 생체고분자물질의 농도를 총유기탄소분석기(TOC- VCSH TOC/TN analyzer; Shimadzu Corp., Japan)를 활용하여 측정하였다. 점토입자 및 응집체에 흡착된 생체고분자물질량(mg-Xanthan Gum/g-kaolinite)은 총 주입된 생체고분자물질량에서 수체 잔존 생체고분자물질의 량을 차감하여 계산하였다.
3. 실험결과 및 고찰
3.1 이온강도가 점토입자-생체고분자물질 응집에 미치는 영향
일반적으로 수체의 이온강도가 증가할수록 부유입자 표면전하 및 정전기적 반발력이 감소하여 응집이 증대되는 것으로 알려져 있다(Partheniades, 2009). 예를 들면, 점토 입자들은 이온강도가 비교적 낮은 하천에서는 부유하지만 이온농도가 높은 하구, 연안에서는 입자간 반발력의 감소로 응집, 퇴적이 활발히 일어난다. 국내 낙동강, 금강 등 대하천 하구에서 점토, 미생물, 입자성 유기물 등 미세 부유입자 응집, 퇴적이 활발히 일어나는 것으로 보고되고 있다(Hwang et al., 2008). 본 연구에서 역시 높은 이온강도가 실험조건으로 적용된 경우, 생체고분자물질과 점토입자의 정전기적 반발력을 감쇄시켜 응집을 증대시키지는 것으로 나타났다.
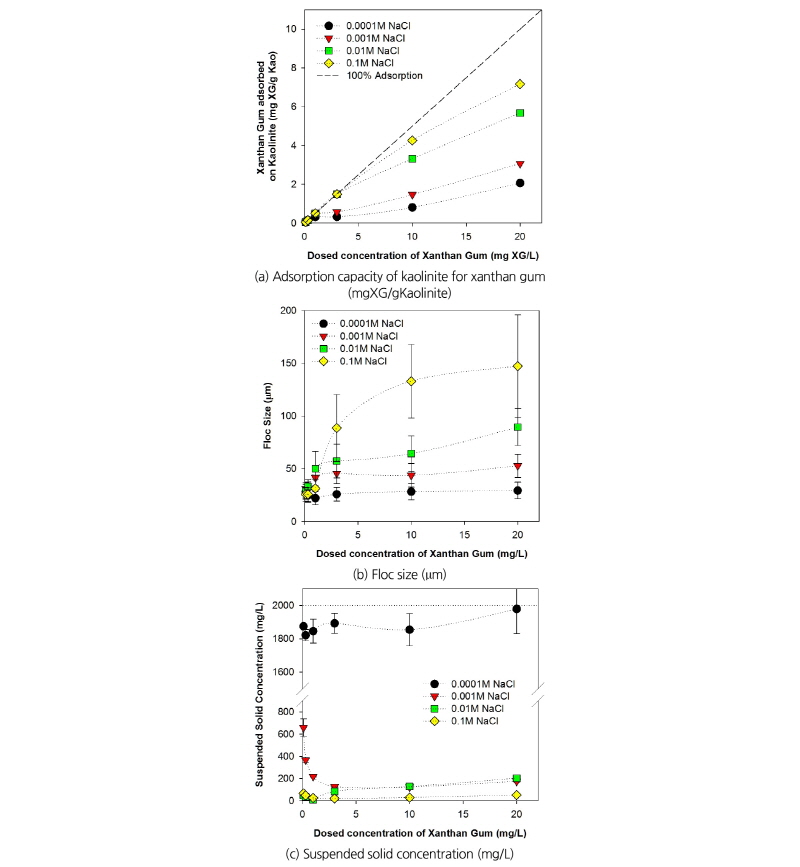
실험에 적용된 현탁액의 점토입자(Kaolinite), 생체고분자물질(Xanthan Gum) 모두 음전하를 띠어 상호간 정전기적 반발력을 가지므로, 생체고분자물질이 점토입자에 흡착하는 량은 크지 않다(Fig. 3(a)). 특히, 본 연구에서의 0.0001 M NaCl 조건과 같이 이온강도가 아주 낮은 경우, 점토입자에 대한 생체고분자물질 흡착량이 2.0 mgXG/gKaolinite 이하로 아주 낮게 나타났다. 하지만, 이온강도가 0.001, 0.01, 0.1 M NaCl로 증대됨과 함께 생체고분자물질 흡착량이 점차 증대되어, 0.1 M NaCl에서 7.0 mgXG/gKaolinite 로써 0.0001 M NaCl 조건에 비하여 3배 이상 증가한 것으로 나타났다. 높은 이온강도에서는 점토입자, 생체고분자물질 간 정전기적 반발력을 감쇄시켜 흡착을 증대시킨 것으로 판단된다. 점토입자의 생체고분자물질에 대한 흡착량 증대가 응집에 미치는 영향은 아래에 구체적으로 기술된다.
생체고분자물질 흡착량이 가장 작게 나타난 0.0001M NaCl 이온강도 실험조건에서는 20 µm 이상 크기의 응집체 형성이 거의 이루어지지 않았고, 1시간 침강 후 잔존하는 부유고형물의 농도가 실험초기 주입농도인 2000 mg/L에 근접하는 것으로 나타나 대부분 점토입자가 응집, 침강하지 않고 부유하는 것으로 나타났다(Figs. 3(b) and 3(c)). 이는 이온강도가 낮으면 점토입자 표면하전 및 정전기적 반발력 증대로 응집이 감소한다는 콜로이드 화학의 일반적인 이론을 잘 따르고 있다(Chassagne et al., 2009; Mietta, 2010). 이에 반하여, 이온강도가 0.0001에서 0.001, 0.01, 0.1 M NaCl로 점차 증대되는 경우 입자간 정전기적 반발적의 감소로 인하여, 응집체가 커지고 입자 응집, 침강 증대로 부유고형물의 농도가 낮아지는 것으로 나타났다.
Fig. 3(b)에 나타난 생체고분자물질 주입량에 따른 응집체 크기 변화를 살펴보면, 생체고분자물질의 주입량이 증가할수록 초기에는 응집체 크기가 급격히 증가하지만, 일정 주입량 이상이 되면 더 이상의 크기 변화가 없는 것으로 나타났다. 생체고분자물질이 점토입자 표면에서 흡착량이 포화된 경우, 생체고분자물질의 추가적인 주입이 응집 증대에 큰 영향을 미치지 않은 것으로 판단된다. 또한, 앞서 언급한 바와 같이, 이온강도가 0.0001에서 0.001, 0.01, 0.1 M NaCl로 점차 증대되면서 생체고분자물질의 점토입자로의 흡착량 증대와 함께 응집체의 크기가 증대되는 것으로 나타났다. 하천 및 호소 조건과 유사한 0.001 M NaCl 이온강도 조건에서는 입자크기가 최대 52.7 µm로 파악되었고, 하구 및 연안 조건과 유사한 0.1 M NaCl 이온강도 조건에서는 응집체의 크기가 최대 148.3 µm까지 증대되는 것으로 나타났다. 이는 하구나 연안에 더 큰 점토질 응집체를 형성하고 퇴적층을 형성하는 일반적인 현상을 증명한다(Partheniades, 2009).
이온강도 증가에 따라 점토입자-생체고분자물질 응집체 크기가 증가하지만, 부유고형물농도는 응집, 침강에 의해 감소하는 것으로 나타났다(Fig. 3(c)). 0.0001M NaCl 이온강도 조건에서는 부유고형물 농도가 초기 점토입자 주입농도와 큰 차이가 없어 응집이 일어나지 않은 것으로 나타났고, 이는 생체고분자물질이 점토입자 표면에 흡착이 되더라도 점토입자가 가교를 형성할 정도의 정전기적 반발력 저감을 이뤄내지 못 한 것으로 판단된다. 하지만, 0.001, 0.01, 0.1 M NaCl로 이온강도가 증대되면서 부유고형물농도가 급격히 저감됨을 알 수 있다. 특히, 0.01, 0.1 M NaCl 이온강도 조건에서는 부유고형물농도가 100 mg/L 이하로 아주 낮게 유지됨을 알 수 있고, 대부분 점토입자는 생체고분자물질과 결합하여 응집체를 형성하고 바닥면으로 침강됨을 알 수 있었다.
3.2. 2가 양이온이 점토입자-생체고분자물질 응집에 미치는 영향
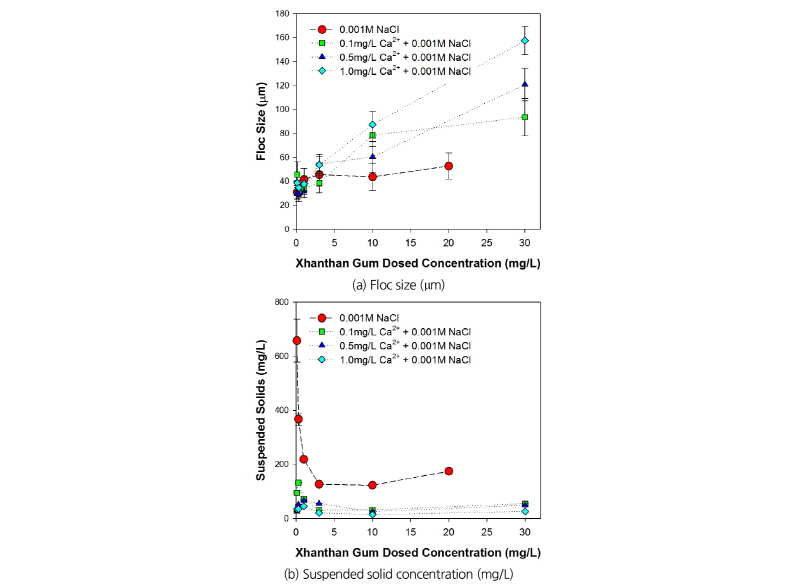
일반적으로 Ca2+와 같은 2가 양이온의 경우, 점토입자-생체고분자물질 간 그리고 생체고분자물질 상호 간 가교를 형성하여 응집을 증대시키는 것으로 알려져 있다(Miatta, 2010; Lee et al., 2012) (Fig. 6). 본 연구에서도 이와 유사하게, Ca2+가 존재하는 경우 응집체 크기가 증가하고 부유고형물농도가 감소하여 응집이 증대되는 것으로 나타났다. Fig. 4(a)에 나타난 바와 같이, 0.001 M NaCl 이온강도 조건에 Ca2+를 추가적으로 주입하는 경우, 생체고분자물질 주입량 증가와 함께 응집체 크기가 크게 증대됨을 알 수 있었다. Ca2+의 주입량이 0.1 mg/L로써 상대적으로 낮은 경우, 생체고분자물질이 일정 주입량 이상이 되면(10 mg/L 이상) 응집체 크기는 크게 변화하지 않는 것으로 나타났다. Ca2+ 주입 없이 이온강도만 증대시킨 경우의 응집체 크기 변화의 경향과 유사하게 나타났다. 하지만, 0.5, 1.0 mg/L Ca2+ 주입량에 대해서는 생체고분자물질 주입량 증가와 함께 응집체크기가 지속적으로 커지는 경향을 나타냈다. 이를 고려하면, 2가 양이온이 수체에 충분히 존재하면, 점토입자-생체고분자물질 사이의 가교를 지속적으로 형성하고 응집을 증대시키는 것으로 판단된다. 부유고형물농도의 경우(Fig. 4(b)), 모든 Ca2+ 주입조건에 대하여 생체고분자물질 주입량 증대와 함께 부유고형물농도가 100 mg/L 이하로 아주 낮게 유지되는 것으로 나타났다. 따라서, 2가 양이온이 수체에 소량 존재하기만 하더라도 응집이 크게 향상될 수 있고, 2가 양이온 농도가 증대될수록 점토입자-생체고분자물질 혹은 생체고분자물질 간 가교를 지속적으로 형성하여 응집을 크게 증대시키는 것으로 판단된다(Plach et al., 2011; Lee et al., 2012).
3.3 휴믹물질이 생체고분자물질-부유입자 응집에 미치는 영향
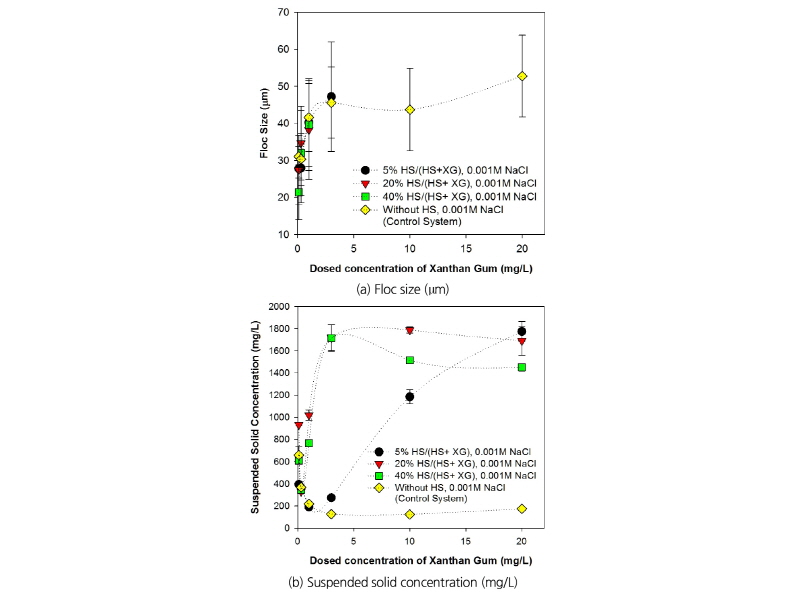
휴믹물질은 점토입자에 흡착될 경우 일반적으로 응집을 감소시키는 것으로 알려져 있다. 수자원환경에서의 수중유기물은 생체고분자물질과 휴믹물질이 혼합되어 있고, 강우, 녹조 등 계절적 요인에 따라 이들 조성이 변화하는 것으로 보고된 바 있다(Bade et al., 2007; Rautio et al., 2011; Lee et al., 2017). 따라서 본 연구에서는 실제 수자원환경에서의 수중유기물 조성과 유사하게 생체고분자물질과 휴믹물질을 일정 비율(5, 20, 40% HA)로 혼합하였고, 이를 점토입자 현탄액에 주입 후 응집실험을 수행하여 휴믹물질 혼합 비율이 응집에 미치는 영향을 파악하고자 하였다. 휴믹물질 없이 생체고분자물질만을 주입한 응집실험의 경우(Control System in Fig. 5), 생체고분자물질 주입농도가 증가할수록 응집능이 증대되고 최대값에 수렴하는 형태로 나타났다. 하지만, 휴믹물질/생체고분자물질 혼합액을 주입한 경우, 주입농도가 낮은 경우 응집이 증가하였으나, 주입농도가 일정값 이상이 되면 응집체 형성이 전혀 이루어지지 않았다.
휴믹물질/생체고분자물질 주입에 따른 응집체 크기 변화의 경향을 자세히 살펴보면(Fig. 5(a)), 휴믹물질이 포함한 실험군에서 휴믹물질/생체고분자물질 주입농도 증가와 함께 응집체 크기가 증가하지만, 일정농도 이상이 되면, 응집체 형성이 전혀 이뤄지지 않은 것으로 나타났다. 예를 들어, 5 % HA를 포함한 경우 휴믹물질/생체고분자물질 주입농도가 3 mg/L 이상이 되면, 그리고 20, 40 % HA를 포함한 경우 주입농도가 1 mg/L 이상이 되면, 응집체가 전혀 형성되지 않아 그래프에 응집체 크기 정보를 표지할 수 없었다. 이와 더불어, 휴믹물질/생체고분자물질 주입에 따른 잔존 고형물 농도 변화의 경향을 살펴보면(Fig. 5(b)), 5 % HA를 포함한 경우 휴믹물질/생체고분자물질 주입농도가 3 mg/L 이상이 되면, 그리고 20, 40 % HA를 포함한 경우 주입농도가 0.3 mg/L 이상이 되면, 잔존 부유고형물농도가 급격히 증가하는 것으로 나타났다.
휴믹물질/생체고분자물질 주입농도 증가는 수체의 휴믹물질 총량 증가를 의미하는 바, 휴믹물질에 수체에 다량 존재할 경우 생체고분자물질의 존재여부와 무관하게 응집체 크기 감소 및 잔존 부유고형물농도 증가 등 응집능의 급격한 감소를 일으키는 것으로 판단된다. 본 실험결과는 강우 시 휴믹물질의 급격한 유입으로 인한 응집능 저하가 보고된 기존 현장관측 연구결과를 뒷받침하고 있다(Lee et al., 2017). 분자량이 상대적으로 작은 휴믹물질은 생체고분자물질에 비해 점토입자로의 흡착이 우세하게 일어나지만, 점토입자의 정정기적 반발력의 영향을 벗어날 만큼 분자량이 충분히 크지 않아 오히려 입자를 안정화시키고 응집을 저하시키는 역할을 하는 것으로 판단된다.
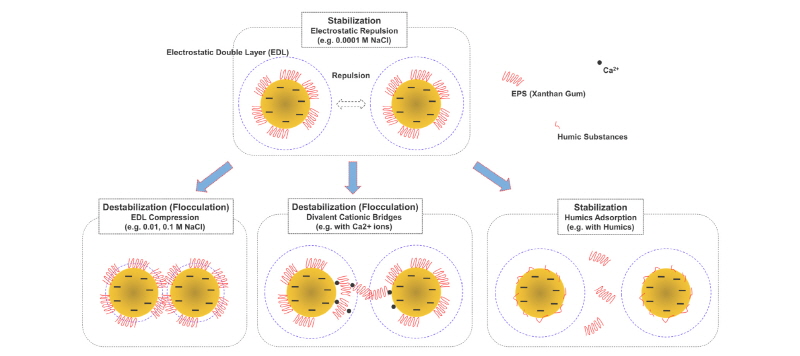
본 연구의 결과를 바탕으로 Fig. 6에 점토입자-생체고분자물질 현탁액에서 일어날 수 있는 응집현상의 모식도를 제시하였다. 수체 이온강도가 지극히 낮은 경우, 예를 들어 본 연구의 0.0001 M NaCl 이온강도를 가지는 경우, 표면전하의 영향이 강하여 점토입자는 음전하를 띠고 정전기적 반발력을 강하게 가지게 되어 입자는 수체에서 부유, 안정화된다. 하지만, 3.1절에 소개된 바와 같이 이온강도가 커짐에 따라 표면전하는 용존 이온들에 의해 중화되고 입자간 정전기적 반발력이 크게 감소하게 된다. Stumm and Morgan에 따르면 점토입자 표면전하가 영향을 미치는 구간을 Electrostatic Double Layer (EDL)으로 지칭하는데, 0.01, 0.1 M NaCl과 같이 강한 이온강도의 경우, EDL 압축, 상쇄가 이뤄져 입자간 정전기적 반발력이 줄어들고 점토입자 사이에 생체고분자물질 가교를 형성하여 점토입자들이 응집하도록 한다(Stumm and Morgan, 1996; Partheniades, 2009). 또한, 3.2절에 소개한 바와 같이, 점토입자는 Ca2+와 같은 2가 양이온에 의해 생체고분자물질에 의한 응집이 증대될 수 있다. Ca2+는 점토-Ca2+-고분자 혹은 고분자-Ca2+-고분자 가교를 형성하여 생체고분자물질에 의한 응집체 형성을 도모하게 된다. 또한, 2가 양이온은 가교 형성 외에, 점토입자 표면에 흡착하여 표면전하 및 정전기적 반발력을 저감시켜 점토입자를 불안정화하여 응집을 증진시킬 수 있다(Mietta et al., 2010; Lee et al., 2012).
이에 반하여, 3.3절에 소개한 바와 같이, 수체에 휴믹물질이 존재하는 경우, 점토입자는 오히려 안정화되어, 응집을 감소시키는 역할을 하는 것으로 나타났다. 장기간의 지구-생화학적 과정에 의해 생성되는 휴믹물질 역시 고분자물질이긴 하지만, 생체고분자물질에 비하여 분자량이 비교적 작고 벤젠링을 다수 포함한 형태를 띠고 있다. 분자량이 아주 크고 사슬구조인 생체고분자물질에 비하여, 점토입자에 대한 응집능이 떨어지고, 오히려 입자를 안정화시키는 역할을 하는 것으로 알려져 있다. 음전하를 띤 휴믹물질은 점토입자에 흡착하여 표면전하와 입자간 반발력을 오히려 증대시키는 것으로 알려져 있다(Kretzschmar et al., 1998; Furukawa et al., 2014; Lee et al., 2017). Fig. 6의 모식도에 나타난 바와 같이, 분자량이 비교적 작은 휴믹물질은 점토입자 표면에 생체고분자물질에 비하여 우선 흡착되어, 생체고분자물질의 흡착을 방해하고 입자 표면전하 및 반발력을 증대시켜 점토입자를 안정화하고 응집을 감소시키는 것으로 판단된다. 3.3 절에 소개된 바와 같이, 수체 내 휴믹물질 분율, 농도가 커지면 이와 같은 입자 안정화 현상이 더욱 크게 나타났다.
4. 결 론
수자원환경에서 생체고분자물질이 응집을 통하여 미세 부유입자들을 큰 응집체로 엮고 바닥면으로 침전, 퇴적시키고 수질을 결정하는 아주 중요한 역할을 한다. 하지만, 다양한 수질화학 조건에 대하여 생체고분자물질이 응집을 증진, 혹은 감소시키는 매커니즘에 대해 체계적으로 연구된 바는 없다. 따라서, 본 연구에서는 이온강도, 2가 양이온 농도 및 휴믹물질 분율과 같은 대표적 수질화학 조건들이 제어된 실험조건을 구현하여, 생체고분자물질에 의한 부유입자 응집 매커니즘을 규명하고자 하였다. 본 연구를 통해 밝혀진 생체고분자물질에 의한 응집 매커니즘은 아래와 같이 요약될 수 있다.
1)이온강도 증가는 점토입자 혹은 생체고분자물질 간 정전기적 반발력을 감소시켜 생체고분자물질이 점토입자 간 가교를 쉽고 형성하고 응집을 증대시키도록 한다.
2)2가 양이온은 점토입자-생체고분자물질 혹은 생체고분자물질 상호 간 가교를 형성하여, 즉 점토-Ca2+-고분자 또는 고분자-Ca2+-고분자 가교를 형성하여, 생체고분자물질에 의한 응집을 증진시킨다.
3)휴믹물질은 점토입자 표면에 생체고분자물질에 비하여 우선 흡착되어, 생체고분자물질의 흡착을 방해하고 점토입자의 정전기적 반발력을 증대시켜 응집을 감소시킨다.
수자원환경에서의 응집의 중요성을 고려한다면, 본 연구의 결과는 하천, 호소, 하구, 연안 등 다양한 수자원환경에서 부유입자 및 퇴적물 거동을 이해하고, 더 나아가 수자원환경의 수질, 퇴적물 관련 최적 관리 방안을 도출할 수 있는 기초 자료로 활용될 수 있으리라 판단된다.